
|
|
|
VITAMINELE
Homocisteina plasmatica este un factor, care poate favoriza aparitia aterosclerozei. O parte din vitaminele din complexul B, precum acidul folic, vitamina B6 si vitamina B12 scad nivelul homocisteinei plasmatice si, astfel, este redus riscul de boli cardiovasculare determinate de ateroscleroza.Exista numeroase studii in populatia generala, care dovedesc acest fapt, in special pentru acidul folic. In subpopulatia pacientilor cu insuficienta renala cronica, strategia de scadere a nivelului plasmatic al homocisteinei, folosind vitamine din complexul B, nu este corespunzatoare.
VITAMINELE DIN COMPLEXUL B SI RISCUL DE BOLI CARDIOVASCULARE
Ateroscleroza, manifestata ca boala coronariana, accident vascular cerebral sau boala arteriala periferica este cea mai importanta cauza de deces in Europa si America de Nord. Se dezvolta insidios pe parcusul mai multor ani si este, de obicei, avansata la momentul cand apar simptomele de afectare cardiovasculara. Reducerea nivelului de colesterol, evitarea tutunului si controlul hipertensiunii arteriale sunt larg acceptate ca strategii preventive in combaterea aterosclerozei.
Se cunostea ca exista o relatie inversa intre consumul de fructe si legume si incidenta bolile cardiovasulare aterosclerotice si acesta a fost considerat un fenomen de protectie pasiva la populatiile cu o dieta bogata in grasimi. Mai recent, posibilitatea ca fructele si legumele sa fie protectoare in mod direct este din ce in ce mai bine documentata (1).
A fost examinata relatia intre bolile cardiovasculare si aportul de acid folic, vitamina B6 (prezente in cantitati apreciabile in fructe si legume) - pe de o parte - si vitamina B12 (prezenta in special in alimente de origine animala) pe de alta parte.
Acidul folic se gaseste in alimente sub forma de complecsi poliglutamici. Pteroilpoliglutamatii alimentari sufera procese de hidroliza sub influenta α-L-glutamil transferazei, enzima care desface resturile de acid glutamic, rezultand acid pteroilglutamic, adica acid folic disponibil pentru absorbtie intestinala. Acesta este redus, apoi metilat, in cadrul procesului de absorbtie cu formarea de metiltetrahidrofolat, care va fi implicat, in asociere cu vitamina B12, pentru biosinteza ADN (prin donarea unei grupari metil vitaminei B12, rezulta tetrahidrofolat, care in continuare funtioneaza ca acceptor de grupari care contin un atom de carbon) (2).
Acidul folic, vitamina B6 si vitamina B12 sunt implicate in metabolizarea metioninei, unul din cei 20 de aminoacizi din componenta proteinelor umane.
Metionina este un aminoacid esential, care functioneaza ca sursa de sulf-adenozil-metionina (SAM). SAM este un donor de grupari metil in lantul de biosinteza a unor numeroase componente celulare, cum ar fi ADN, ARN, creatina, proteine si catecolamine.
Prin demetilarea SAM se formeaza homocisteina. Nivelul homocisteinei serice variaza in functie de cele 2 cai de metabolizare ale ei. Prima ar fi trans-sulfurarea la cisteina, prin intermediul enzimei cistation b-sintetaza, enzima care necesita vitamina B6 drept cofactor. A doua cale ar fi remetilarea la metionina necesitand prezenta unor enzime, care au co-substrat acidul folic si co-enzima vitamina B12 (1).
Nivelul homocisteinei in sange este invers proportional cu nivelul plasmatic al folatilor, vitaminei B12 si piridoxal 5-fosfatului (vitamina B6), implicit este invers proportional cu aportul exogen al acestor vitamine.
Se pune problema, care este concentratia normala a homocisteinei serice.
Hiperhomocisteinemia este definita ca un nivel plasmatic al homocisteinei mai mare de 15 mmol/L, desi niveluri de peste 10 mmol/L par sa aiba efecte nocive pentru indivizii cu boala coronariana si ateroscleroza, asa cum se va arata ulterior in acest articol (3). Nivelul seric al homocisteinei incepe sa creasca, daca nivelul seric al folatilor scade la 20-25 nmol/L. Se poate spune ca nivelul homocisteinei este un marker foarte sensibil al statusului folatilor, acesta crescand cu mult inaintea aparitiei deficitului manifest de folati. Cresteri ale cantitatii de folati din dieta de la 0,5 la 5 mg zilnic s-a demonstrat ca reduc nivelul seric al homocisteinei cu o valoare, care in medie reprezinta un sfert din valoarea homocisteinei serice dinainte de interventia asupra dietei, asa cum a aratat o metaanaliza, care a inclus 12 studii randomizate controlate (4).
Se stie ca homocisteina favorizeaza aparitia si dezvoltarea aterosclerozei. Sunt multe teorii cu privire la mecanismul exact al acestui fenomen. Unii sugereaza ca gruparea sulfidril din molecula homocisteinei este implicata deoarece este usor oxidabila. Au fost elaborate teorii, care sa justifice rolul patogenic al homocisteinei, precum favorizarea agregarii plachetare, dezvoltarea leziunilor endoteliale, alterarea afinitatii pentru fibrina a lipidelor si lipoproteinelor, alterari ale proliferarii celulelor musculare netede si cresterea productiei de specii reactive de oxigen, ducand la cresterea stresului oxidativ.
S-a aratat ca homocisteina produce injurii celulare in culturile de celule endoteliale si asupra endoteliului la animalele de laborator si la om. Endoteliul vascular joaca un rol critic in controlul tonusului vascular si, astfel, in reglarea fluxului sanguin. Disfunctia endoteliala vasculara este o prima etapa in dezvoltarea bolii vasculare si contribuie la patogeneza aterosclerozei, inclusiv a bolii coronare. S-a aratat ca disfunctia endoteliala, asa cum este evidentiata prin dilatatia mediata de flux a arterei brahiale, este proportionala cu extensia bolii coronare. Numeroase studii, care folosesc metoda mai sus mentionata, sugereaza ca hiperhomocisteinemia duce la perturbari ale functiei endoteliale. In plus, cresteri cresteri chiar in limite fiziologice ale nivelului plasmatic al homocisteinei, precum cele produse dupa ingestia de metionina, produc astfel de perturbari.
A fost demonstrat ca acidul folic imbunatateste functia endoteliala la adultii sanatosi cu hiperhomocisteinemie. La pacientii cu boala coronariana documentata, scaderea nivelului plasmatic al homocisteinei, prin suplimentarea aportului de acid folic (5 mg/zi) imbunatateste functia vaselor de rezistenta. Se pare ca scaderea nivelului homocisteinei este responsabila de acest efect si nu cresterea nivelului seric al folatului (5).
S-a pus in evidenta prin numeroase studii ca exista o asociere intre cresterea nivelului plasmatic al homocisteinei si bolile cardiovasculare. Trebuie remarcat faptul ca aceasta asociere pare a fi mai puternica in studii caz-control cu o metodologie mai putin pusa la punct, in comparatie cu studiile prospective. Opinia cvasigenerala este ca asocierea dintre nivelul plasmatic al homocisteinei si bolile cardiovasculare este puternica, graduala si independenta de alti factori. Foarte putine opinii sunt pentru faptul ca afectarea cardiovasculara ar fi cauza cresterii nivelului seric al homocisteinei.
S-a incercat sa se demonstreze daca imbogatirea cu acid folic a alimentelor (care ar duce la cresterea aportului zilnic de acid folic cu 0,2 mg/zi) sau aportul de acid folic pe cale medicamentoasa (de aproximativ 2 mg/zi) are eficienta mai mare asupra scaderii nivelului seric al homocisteinei (6, 7, 8). Indivizii care obtin beneficiul cel mai mare de pe urma suplimentarii aportului de acid folic prin oricare din cele doua modalitati mentionate sunt cei cu riscul cel mai mare de boala cardiovasculara, precum pacientii cu istoric de boala ischemica coronariana (9).
Un studiu al grupului numit PACIFIC (Prevention with a Combined Inhibitor and Folic Acid in Coronary Heart Disease) a cuprins un numar de 723 de indivizi cu istoric de infarct miocardic acut sau angina instabila, care au fost recrutati din centre de cardiologie din Australia si Noua Zeelanda si au primit zilnic(in mod aleator) acid folic 2 mg, acid folic 0,2 mg sau placebo. Amandoua dozele de acid folic au redus nivelul seric al homocisteinei dar efectele dozei de 2 mg au fost cu o treime mai mari decat ale dozei de 0,2 mg (o reducere de 1,8 mmol/L, respectiv, de 1,2 mmol/L a homocistinei plasmatice). Concluzia este ca suplimentarea terapeutica a aportului de acid folic are un efect mai pronuntat asupra nivelului seric al homocisteinei, decat imbogatirea alimentelor in acid folic (10).
Intr-un articol aparut in ianuarie 2004, este facuta o statistica a studiilor referitoare la acidul folic si homocisteina plasmatica la pacientii cu boala coronariana. In 22 din 27 studii retrospective caz-control, pacientii cu boala coronariana au avut o concentratie semnificativ crescuta a nivelului homocisteinei, fata de subiectii martor (odds ratio = 1,2-10,9, dupa ajustarea in functie de alti factori de risc cardiovasculari). Totusi, numai 4 din 7 studii prospective caz-control au aratat o corelatie intre nivelurile crescute ale homocisteinei serice si infarctul miocardic, respectiv moartea de cauza coronariana.
O metaanaliza a 12 studii randomizate controlate a scos in evidenta ca suplimentarea aportului de folati, impreuna cu vitamina B6 si B12, reduce nivelul plasmatic al homocisteinei. Totusi, consecintele clinice ale acestei interventii sunt necunoscute.
Doua studii randomizate, comparativ cu placebo, despre folati raportand rezultate din punct de vedere clinic au fost finalizate.
Un studiu a analizat suplimentarea folatilor la o populatie cu boala coronariana cunoscuta, stabila si nu a gasit diferente intre lotul tratat si cel care a primit placebo (593 pacienti au primit, fie 0,5 mg/zi acid folic, fie placebo). Rezultatele ("endpoint"-uri) primare al studiului au fost: mortalitatea indiferent de cauza, moartea subita, infarctul de miocard, accidentul vascular cerebral si operatiile chirurgicale majore. Studiul ar fi putut detecta o reducere cu 50% a evenimentelor clinice, bazat pe datele observationale, la pacientii cu boala coronariana. A fost gasita o incidenta a evenimentelor mai sus mentionate de 15% pe un interval de 2 ani. De asemenea, toti pacientii din acest studiu au fost in tratament cu statine inainte de initierea suplimentarii administrarii de folati.
Al doilea studiu a analizat rezultatele administrarii suplimentare de folati la 553 pacienti dupa PCI (percutaneous coronary intervention). Pacientii au fost tratati cu 1 mg de folat plus 10 mg vitamina B6 si 400 mg de vitamina B12 pentru 6 luni dupa PCI. Dupa o medie de 11 luni de urmarire a pacientilor, rata restenozarii necesitand revascularizare a fost mai mica in ramura studiului care a inclus pacientii tratati cu vitamine (9,9 versus 16% rata a restenozarii, risc relativ=0,62; interval de incredere 95%:0,40-0,97, pacienti care au necesitat tratamentul =16). A fost inregistrat si o tendinta nesemnificativa spre scaderea numarului de decese si de infarct miocardic la pacientii tratati cu vitamine la 6 si 12 luni dupa interventie (3).
Alta metaanaliza aparuta intr-un articol publicat in octombrie 2005 a luat in consideratie 25 de studii randomizate incluzand date de la 2 596 de pacienti si care a evaluat efectele asupra concentratiei plasmatice a homocisteinei ale diferitelor doze de acid folic si ale asocierii acidului folic cu vitaminele B12 si B6. Modificarile nivelului plasmatic al homocisteinei au fost mai mari atunci cand s-a pornit de la valori mari ale homocisteinemiei si valori scazute ale nivelului folatilor sanguini; de asemenea, au fost mai mari la femei decat la barbati. La concentratii standardizate de 12 mmol/L homocisteina si 12 nmol/L folati pretratament, doze zilnice de 0,2; 0,4; 0,8; 2 si 5 mg acid folic au fost asociate cu o reducere a homocisteinei in medie cu 13%, 20%, 23%, 23% si, respectiv, 25%. Vitamina B12 (0,4 mg/zi) produce o scadere suplimentara de 7% a homocisteinemiei, dar vitamina B6 nu a avut un efect semnificativ (11).
Vitamina B6 pare sa fie mai putin implicata in scaderea nivelului homocisteinei serice, dar in studiile referitoare la riscul cardiovascular pacientii cu nivel plasmatic crescut de vitamina B6 au un risc de afectare cardiovasculara mai mic decat pacientii cu nivel plasmatic mai mic de vitamina B6 (12).
Luand in considerare studiile care au inclus date despre nivelul seric al folatilor, vitaminei B6 si vitaminei B12 si implicatiile acestora asupra riscului cardiovascular se pot trage urmatoarele concluzii:
1. Exista o relatie inversa intre nivelul seric al folatilor si riscul cardiovascular
2. Riscul pare a fi mediat in parte de cresterea nivelului seric al homocisteinei. Riscul a fost substantial mai mare la fumatori si pacienti hipertensivi si apreciabil crescut la pacienti hiperlipidemici (1). S-a aratat ca o scadere de lunga durata a nivelului plasmatic al homocisteinei cu 1 mmol/L a fost asociata cu o scadere de aproximativ 10% a riscului de boala vasculara (13).
3. O doza de acid folic mai mare sau egala cu 0,8 mg este necesara pentru o scadere optima a nivelului de homocisteina.
4. Relatia inversa intre nivelul plasmatic de vitamina B6 si riscul cardiovascular pare a fi mai puternica, decat cea asociata cu nivelul plasmatic al folatilor, si pare a fi independenta de homocisteina (12).
5. Exista si o asociere inversa intre aportul de vitamina B12, asociat aportului de acid folic, si nivelul seric al homocisteinei (4).
6. Nivelul plasmatic crescut al homocisteinei pare sa fie un factor de risc la fel de puternic pentru boala cardiovasculara atat la femei, chiar si inainte de menopauza, cat si la barbati (1).
Este plauzibil faptul ca homocisteina poate modifica efectul altor factori de risc cardiovasculari cunoscuti. Se pare ca homocisteina actioneaza asupra functiei endoteliale, asupra oxidarii LDL, favorizand coagularea si agregarea plachetara. Prin aceste actiuni, homocisteina poate creste riscul cardiovascular asociat factorilor de risc conventionali.
TRATAMENTUL CU VITAMINE DIN COMPLEXUL B LA PACIENTI CU INSUFICIENTA RENALA CRONICA SI RISCUL DE BOLI CARDIOVASCULARE
Boala vasculara aterotrombotica ramane principala cauza de morbiditate si mortalitate la pacientii cu insuficienta renala cronica, indiferent daca acestia se afla in stadiul preterminal, daca se afla in dializa sau au primit un transplant renal. Cu toata prevalenta inalta a factorilor de risc bine stabiliti pentru bolile cardiovasculare, la pacientii cu insuficienta renala cronica, valoarea lor predictiva nu este la fel de puternica, ca la populatia generala. Managementul diabetului, hipertensiunii arteriale sau dislipidemiei este frecvent inadecvat si pare sa fie insuficient, pentru a preveni evenimentele cardiovasculare la acesti pacienti.
In ultimii 15 ani, homocisteina a fost recunoscuta ca predictor independent al riscului de boala cardiovasculara, nu numai in populatia generala, asa cum s-a descris mai sus, dar si la pacientii cu insuficienta renala cronica.
In consecinta, au aparut studii care au folosit diferite metode de tratament pe baza de folati si au fost testat potentialul lor de a scadea nivelul plasmatic al homocisteinei la grupa de pacienti mai sus mentionata. Insa, in contrast cu rezultatele obtinute in hiperhomocisteinemie la populatia generala, hiperhomocisteinemia la pacientii cu insuficienta renala s-a dovedit a fi refractara la suplimentarea aportului vitaminelor din complexul B inclusiv de acid folic.
Aceasta rezistenta la acidul folic ar fi in parte determinata de unele defecte ale metabolizarii acestuia, defecte care apar la cei cu insuficienta renala cronica. Astfel, au fost descrise tulburari de absorbtie ale metiltetrahidofolatului, scaderea activitatii α-L-glutamil transferazei-enzima, care scindeaza poliglutamatii-, blocarea inglobarii gruparilor metil ale metiltetrahidrofolatului in acizi nucleici sau proteine (din cauza unor anioni retinuti la pacientii cu insuficienta renal cronica); de asemenea, reducerea nivelurilor serice ale folatilor liberi disponibili pentru transportul transmembranar, din cauza unei legari crescute de proteinele plasmatice.
Un numar mare de studii au avut drept tinta normalizarea nivelului homocisteinei prin suplimentarea aportului de folati la pacienti cu infuficienta renala cronica. S-a considerat ca administrarea de doze suprafiziologice de folati ar duce la cresterea proportiei de homocisteina, care va fi remetilata, reducand astfel excesul de homocisteina. De asemenea, dozele mari de folati ar fi necesare pentru a corecta defectele de metabolizare ale acidului folic mai sus mentionate.
Nivelul plasmatic al homocisteinei, ca punct de plecare in studiile privind eficacitatea acidului folic, a depins si de pretratamentul cu preparate multivitaminice, care contin acid folic, vitamina B6 si vitamina B12, situandu-se la pacientii supusi dializei la valori intre 20 si 50 mmol/L. La pacientii cu insuficienta renala preterminala si la cei care au primit un transplant renal, nivelurile plasmatice ale homocisteinei se situeaza intre 15 si 20 mmol/L, depinzand de gradul de insuficienta renala. Comparand cu tratamentul cu placebo, cu tratamentul cu doze standard de folati (0,4 mg/zi) sau cu lipsa interventiei terapeutice, tratamentul cu doze suprafiziologice de folati duce la scaderi mai importante ale nivelului homocisteinei. Se obtine, in general, o scadere a homocisteinemiei de aproximativ 30%, putine raportari aratand o scadere de 60-70% Pacientii, care au avut concentratia cea mai mare a homocisteinei plasmatice, au beneficiat cel mai mult de tratament. Totusi, doar o mica parte din pacientii cu insuficienta renala cronica sub dializa au ajuns la un nivel plasmatic normal al homocisteinei, daca se accepta ca limita superioara a concentratiei normale a homocisteinei ar fi de 15 mmol/L. Insa, daca se ia in consideratie faptul ca si concentratii serice de 12-14 mmol/L ale homocisteinei sunt asociate cu cresterea riscului de boala cardiovasculara, practic, nici un pacient aflat in dializa nu ajunge post-tratament la nivelurile normale ale homocisteinei. Regimurile de tratament cu folati la pacientii aflati in predializa si la primitorii de transplant renal au dus insa la scaderi ale nivelului plasmatic al homocisteinei la valori sub 12 mmol/L la 20% din pacientii in predializa si la 65% din primitorii unui transplant renal.
Doza necesara pentru a obtine o scadere maximala a homocisteinei serice este un subiect de dezbatere. Doua studii efectuate la pacienti aflati in dializa au aratat ca o doza de acid folic de 15 mg/zi duce la o scadere aditionala cu 15-25% a homocisteinei totale, comparativ cu doza de 1 mg. Alte cateva studii nu au gasit un astfel de beneficiu.
Se sugereaza ca exista o limita superioara (care este de 5 mg folati/zi) peste care nu poate functiona suplimentar remetilarea homocisteinei si, astfel, reducerea nivelului plasmatic al acesteia. Doza optima de acid folic ar fi cuprinsa in intervalul 1-5 mg/zi.
Referitor la vitamina B6, un studiu randomizat a aratat ca suplimentarea aportului acestei vitamine reduce nivelul plasmatic al homocisteinei la proba de incarcare cu metionina la pacientii cu insuficienta renala. Adaugarea de vitamina B12 nu a adus beneficiu suplimentar la pacientii primitori ai unui transplant renal, dar s-a dovedit eficace in scaderea hiperhomocisteinemiei (cu 35%) la pacientii in dializa care aveau niveluri scazute ale cobalaminei.
Nu au fost finalizate sau inca nu au fost raportate rezultatele unor studii care sa arate clar beneficii clinice ale tratamentului hiperhomocisteinemiei la pacienti cu insuficienta renala cronica (14).
CONCLUZII
Suplimentarea aportului de acid folic este o metoda ieftina si cu eficacitate mare in reducerea nivelului seric al homocisteinei. Daca studii pe populatii mari cu risc crescut de evenimente cardiovasculare vor putea fi facute, folosind strategii de reducere a riscului de evenimente cardiovasculare, prin scaderea nivelului seric al homocisteinei, aceste strategii ar putea avea implicatii importante pentru sanatatea populatiei. S-ar putea folosi doze mai mari de acid folic (ca medicament), care sa scada nivelul homocisteinei serice la indivizii cu risc crescut de afectare cardiovasculara, iar concentratia medie a homocisteinei la populatia totala ar putea fi redusa prin imbogatirea alimentelor in acid folic. Asocierea la acidul folic a suplimentarii aportului de vitamina B6 si B12 ar putea aduce un beneficiu suplimentar (insa unul mic).
In unele tari, precum SUA, s-a introdus imbogatirea fainii in acid folic pentru prevenirea defectelor de tub neural (lipsa de acid folic este teratogena pentru sistemul nervos), ceea ce complica evaluarea beneficiului sau a eventualelor riscuri ale scaderii nivelului plasmatic al homocisteinei in bolile cardiovasculare.
Pacientii cu insuficienta renala preterminala, in dializa, sau primitorii unui transplant renal au un risc cardiovascular crescut, mediat in parte de cresterea nivelului homocisteinei. Strategiile de reducere a nivelului homocisteinei nu sunt insa foarte eficace, mai ales la pacientii aflati sub dializa.
Homocisteina - colesterolul anilor '90 Homocisteina, produs intermediar al metabolismului metioninei, reprezinta astazi un factor de risc cardiovascular recunoscut, motiv pentru care a fost denumita si 'colesterolul anilor '90'. Ipoteza ca hiperhomocistinemia este un factor de risc cardiovascular a fost propusa in urma cu 30 de ani de catre McCully, care a observat leziuni vasculare la copii cu homocisteinurie. Aceasta este o boala rara, autozomal recesiva, determinata de scaderea activitatii cistationin-B-sintetazei, caracterizata prin nivel crescut al homocisteinei in sange, prezenta homocisteinei in urina, alaturi de defecte ale scheletului, retard mental, dislocatie de cristalin. ()
Din punct de vedere biochimic, colina participa la
reactiile de transmetilare ca donoare si acceptoare de grupari
metil. Transmetilarile au loc sub influienta unor enzime numite
transmetilaze. Colina prin donare de metil se transforma in betaina.
Colina este o forma de protectie a betainei exogene si
totodata o sursa de betaina. Homocisteina prin
acceptarea unui metil de la colina trece in metionina (trecerea
homocisteinei in metionina se face cu consum de colina).
Colina, betaina,
metionina si chiar acetilcolina favorizeaza biosinteza
fosfolipidelor in ficat pe care apoi le pun in circulatie. In
absenta acestor subsatnte ficatul se infiltreaza cu
grasimi (steatoza hepatica). Lipidele infiltrante provin in
principal din neogeneze, avand drept surse primare glucidele.
Colina are asupra
colesterolului o actiune oxidativa (degradanta).
SINERGICI SI ANTAGONISTI
Cei 20 de aminoacizi naturali constituie alfabetul proteinelor.Distributia lor calitativa si cantitativa intr-o proteina determina caracteristicile chimice,valoarea ei nutritiva si functiileei metabolice in organism.Dintre cei 20 de aminoacizi uzuali,organismul uman si al vertebratelor superioare poate sintetiza un numar limitat,restul trebuie sa fie furnizati zilnic prin hrana si se numesc aminoacizi esentiali !9!.Cei mai multi autori, considera drept aminoacizi esentiali urmatorii:valina,fenilalanina,metionina,lisina,triptofanul; altii, includ si leucina,izoleucina ,treonina si histidina!1,3,5,6,7,8,9,12!.
In cazul biosintezei metioninei se realizeaza transferul gruparii metil de la N-5-CH3-FH4 la homocisteina.
In procesul de biosinteza a metioninei se produce neogeneza grupei metil si nu transferul acesteia de la alti donori. Metionina are rol insemnat in formarea colinfosfolipidelor deoarece grupele metil din colina provin din metionina activata (S-adenozilmetionina).
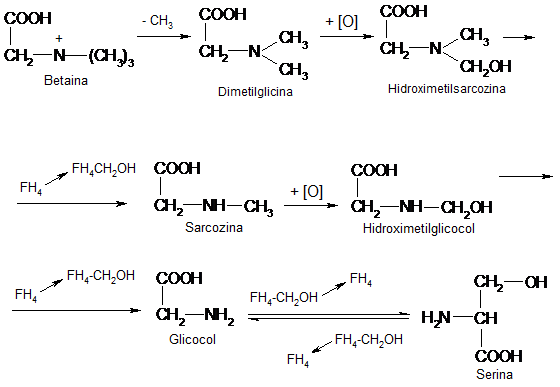
Dintre reactiile la care participa N-10-formil-FH4 si N-10-CH2OH-FH4,e importanta trasformarea betainei in serina.
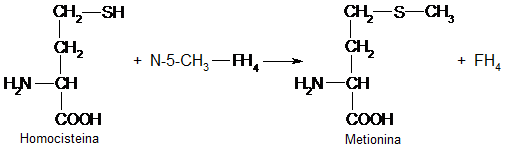
BIBLIOGRAFIE SELECTIVA
1. Graham IM, O'Callaghan P - Vitamins, homocysteine and cardiovascular risk. Cardiovasc Drugs Ther, 2002 Sep;16(5):383-9.
2. Stroescu V - Bazele farmacologice ale practicii medicale, Ed Medicala,1998, pag 457-458.
3. Kerri Hecox si colab. - Is folate supplementation indicated for patients with CAD? Journal of Family Practice, January 2004 . Vol. 53, No.1.
4. Homocysteine Lowering Trialists' Collaboration. Lowering blood homocysteine with folic acid based supplements: meta-analysis of randomised trials. BMJ, 1998; 316: 894-8.
5. Stanger O si colab. - Effects of folate treatment and homocysteine lowering on resistance vessel reactivity in atherosclerotic subjects. J Pharmacol Exp Ther, 2002 Oct;303(1):158-62.
6. Malinow M si colab. - Reduction of plasma homocyst(e)ine levels by breakfast cereal fortified with folic acid in patients with coronary heart disease. N Engl J Med, 1998; 338: 1009-15.
7. Brouwer I si colab. - Low-dose folic acid supplementation decreases plasma homocysteine concentrations: a randomised trial. Am J Clin Nutr, 1999; 69: 99-104.
8. Appel L si colab. - Effect of dietary patterns on serum homocysteine: results of a randomised, controlled feeding study. Circulation, 2000; 22: 852-7.
9. MacMahon S - Blood pressure and the risk of cardiovascular disease. N Engl J Med, 2000; 342: 50-2.
10. Neal B si colab. - PACIFIC Study Group. Dose-dependent effects of folic acid on plasma homocysteine in a randomized trial conducted among 723 individuals with coronary heart disease. Eur Heart J, 2002 Oct;23(19):1509-15.
11. Homocysteine Lowering Trialists' Collaboration. Dose-dependent effects of folic acid on blood concentrations of homocysteine: a meta-analysis of the randomized trials. Am J Clin Nutr, 2005 Oct;82(4):806-12.
12. Eikelboom JW si colab. - Homocyst(e)ine and cardiovascular disease: A critical review of the epidemiologic evidence. Ann Intern Med, 1999;131:363-375.
13. Boushey CJ si colab. - A quantitative assessment of plasma homocysteine as a risk factor for vascular disease: probable benefits of increasing folic acid intakes. JAMA, 1995; 274: 1049-57.
14. De Vriese
AS si colab. - Is folate a promising agent in the prevention and treatment of
cardiovascular disease in patients with renal failure?
Kidney Int, 2002 Apr;61(4):1199-209.