
|
|
|
Istoric
Anilina a fost obtinuta pentru prima data la Unverdorben in 1826 prin distilarea uscata a indigoului si a fost denumita krystallin. In 1834, Runge izoleaza anilina din gudronul de carbune, respectiv din fractia de ulei usor(80-170 C) si o denumeste kyanol. Denumirea de anilina, din numele spaniol al indigoului(anil), a fost data de Fritzsche in 1840, care a preparat-o prin tratarea indigoului cu hidroxid de sodiu. Prima sinteza a anilinei a fost facuta de Zinzin in 1842 prin reducerea nitrobenzenului cu sulfura de amoniu. In 1843, Hofmann a dovedit ca in toate procedeele mentionate se obtine unul si acelasi produs- anilina. In 1856, Perkin, atunci in varsta de 18 ani, obtine primul colorant sintetic- mauvelina- prin oxidarea sulfatului de anilina. Fabricarea industriala a anilinei a inceput in 1857.
 Proprietati fizice si formula
Proprietati fizice si formula
NH2

Metode de preparare
Principalele metode industriale de preparare ale anilinei sunt:
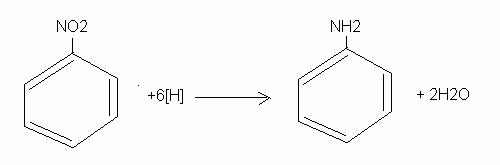
reducerea nitrobenzenului cu hidrogen obtinut din reactia acidului clorhidridric cu metalele, folosindu-se catalizator de cupru(ca la Fagaras) ;
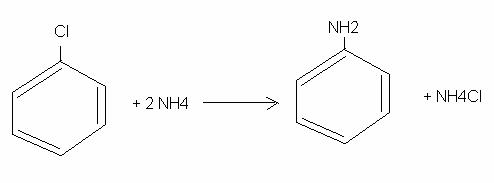
alchilarea amoniacului cu derivati halogenati ;
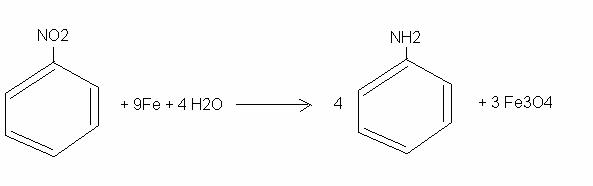
reducerea nitribenzenului cu pilitura de fier, folosindu-se ca electroliti saruri de fier(clorura, sulfat, acetat, formiat) care se pot obtine in vasul de reducere, prin adaugarea de acizi in cantitati mici inainte de adaugarea nitrobenzenului ;
Proprietati chimice
1) Solubilitatea si constanta de bazicitate
In solutie, anilina ionizeaza ca si amoniacul, acceptand protoni pe care ii fixeaza laperechea de electroni neparticipanta a atomului de azot printr-o legatura covalent coordinativa :
 In cazul anilinei, capacitatea de fixare a
protonului scade, deci bazicitatea se reduce(3,8 x 10-10) si de aceea anilina nu se dizolva complet
in apa.
In cazul anilinei, capacitatea de fixare a
protonului scade, deci bazicitatea se reduce(3,8 x 10-10) si de aceea anilina nu se dizolva complet
in apa.
Anilina se dizolva, insa, complet in solutie de acid clorhidric, deoarece se formeaza un compus ionic, solubil in apa :

2) Reactia de alchilare - cu derivati halogenati

3) Reactia de acilare- cu acid acetic

4) Reactia de diazotare
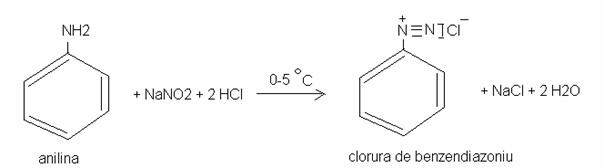
5) Reactia anilinei(vapori) cu acetilena

6) Identificarea
Anilina+hipoclorit de calciu violet
Anilina+permanganat de potasiu : verde si apoi in negru (negru de anilina).
Utilizari
Anilina se utilizeaza in numeroase ramuri ale industriei chimice de sinteza organica, fiind printre materiile prime fundamentale. Anilina se utilizeaza la fabricarea de coloranti; negrul de anilina este unul dintre cei mai buni coloranti negri pentru fibre. Din anilina se fabrica cca. 40 de coloranti de larga circulatie, la care se adauga numerosi alti produsi fabricati din diversi derivati de anilina. Printre intermediarii cei mai importanti preparati din anilina ca materie prima sunt dimetilanilina, acetanilida si chinaldina. Numeroase medicamente din clasa sulfamidelor se prepara folosind anilina si derivati ai ei ca materie prima. Condensarea anilinei cu acetona conduce la unul din cei mai utilizati antioxidanti, fabricat in tara printr-un proces original.
Anilina mai este folosita la fabricarea acceleratorilor de vulcanizare si a unor materiale plastice. Derivatul ei acetilat, acetanilida, numita si antifebrina are proprietati antipiretice.