
|
|
|
Din punct de vedere al catalizei eterogene, o reactie parcurge mai multe etape, astfel ca reactantii, in urma accesului in structura, trebuie sa difuzeze pana in spatiile cu proprietati catalitice si sa se adsoarba. In aceasta situatie, se formeaza un intermediar activat care apoi reactioneaza spre produsii finali, care se desorb si trebuie sa poata difuza prin pori spre exteriorul structurii. Spre deosebire de alti catalizatori, zeolitii, datorita structurii cristaline pot adsorbi sau nu mai multe molecule. Zeolitii cu pori mici au o selectivitate geometrica "pura" in sensul ca nu au acces in interiorul porilor decat molecule mici, iar cei cu pori mari au o selectivitate mixta, adica dintr-un amestec de substante nu sunt adsorbite decat cele care intra in pori dar, dintre acestea sunt retinute doar cele mai polare. In afara de selectivitatea geometrica pura, mai exista si o selectivitate datorata diferentelor de difuzie a unor reactanti in si din porii catalizatorului. Pentru a explica acest aspect, s-a introdus notiunea de difuzie configurationala, care se produce atunci cand dimensiunea critica a moleculei ce difuzeaza este foarte apropiata de dimensiunea porilor zeolitului. In acest caz intervine nu numai dimensiunea moleculei ci si "dinamica" acesteia, respectiv posibilitatile de orientare spatiala, in anumite conditii.
Accesul moleculelor
reactante si probabilitatea formarii moleculelor de produs sunt
determinate in principal de dimensiunile dar si de configuratia
moleculelor (selectivitate de forma). Termenul de selectivitate de
forma a fost introdus de catre Weisz si Frillete pentru a
descrie comportarea neasteptata a zeolitului LTA schimbat ionic cu Ca2+
( CaA); la 260
In tabelul III.1 este prezentat un scurt istoric al catalizei selective de forma. Se pot distinge mai multe tipuri de selectivitate de forma, depinzand fie de dimensiunea limita a ferestrei de acces in pori a moleculei de reactant, fie de posibilitatea eliminarii din pori a produsului de reactie, fie de posibilitatea aparitiei anumitor stari de tranzitie.
Tabelul III.1. Scurt istoric al catalizei selective de forma.
|
1925 - primul efect de sita moleculara (adsorbtia pe chabazit; 1932 - sita moleculara - material poros care actioneaza ca sita la scara moleculara; 1960 - cataliza selectiva de forma pe site moleculare; 1966 - termenul de cataliza selectiva de forma apare in Enciclopedia of Chemistry; 1968 - primul proces comercial selectiv de forma Selectoforming pe erionit natural; 1967 - sinteza
zeolitului ZSM-5 la firma Mobil Oil face posibila punerea in
practica a mai multor procese selective de forma ( 1968 - selectivitatea de stare de tranzitie; 1970 - efectul concentratie reactantilor in porii catalizatorilor zeolitici, 1984 - efectul "cuibar" - efectul "capcana"; 1991 - cataliza la gura porilor; 1995 - mecanism de tip "cheie - broasca" |
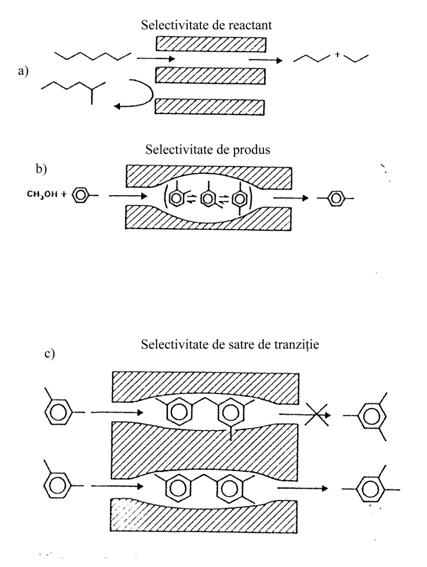
Selectivitatea reactantului apare atunci cand numai o parte din moleculele reactante sunt suficient de mici pentru a putea difuza in porii catalizatorului (fig. III.3.a).
Selectivitatea la eliminarea produsului apare atunci cand o parte din produsii formati in pori sunt prea voluminosi si nu pot difuza afara din pori, nefiind observati ca produsi eliminati (fig.III.3.b)
Selectivitatea restrictiva a starii de tranzitie apare cand anumite reactii sunt impiedicate deoarece starile de tranzitie corespunzatoare ar avea nevoie de mai mult spatiu decat cel disponibil in cavitati (fig. III.3.c).
Controlul traficului molecular apare in zeolitii cu mai mult de un sistem de canale. In acesti zeoliti, reactantul este admis preferential in pori printr-un sistem de canale iar produsii sunt eliminati prin alt sistem de canale. Contra - difuzia este astfel minima (fig.III.3.d).
Conceptul de selectivitate de stare de tranzitie fost propus de catre Csicsery pentru a explica de ce nu se formeaza trialchilbenzeni simetrici in cazul disproportionarii dialchilbenzenilor pe H-MOR, desi difuzia acestora prin porii catalizatorului poate avea loc. Odata cu descoperirea zeolitilor cu pori medii si in special a zeolitului ZSM-5 cercetarile in domeniul catalizei selective de forma pur si simplu au "explodat", aplicatiile catalizei pe zeoliti cunoscand o expansiune extraordinara.
Majoritatea reactiilor catalizate de zeoliti au loc in interiorul porilor si /sau cavitatilor zeolitice intracristaline ale acestora. Cu alte cuvinte catalizatorii zeolitici pot fi considerati ca fiind o succesiune de reactoare nano si /sau moleculare, activitatea, selectivitatea si stabilitatea acestora depinzand intr-o masura mai mare sau mai mica de deschiderile (diametrele) porilor si cavitatilor, selectivitatea de forma fiind o caracteristica generala a acestora.
d)
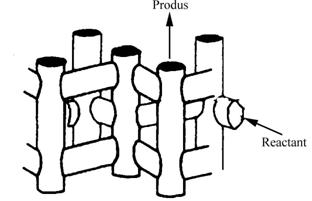
Controlul traficului molecular
Fig. III.3. Cataliza selectiva de forma: a) selectivitate de reactant; b) selectivitate la eliminarea produsului; c) selectivitate restrictiva a starii de tranzitie; d) trafic molecular.
Trebuie subliniat faptul ca, centrele active situate pe suprafata externa a cristalitelor zeolitice, desi sunt prezente intr-un numar mic comparativ cu centrele situate in porii sau cavitatile zeolitice (sub 1 % pentru cristalele de 1 μm lungime) sunt implicate in reactiile catalitice, in general prezenta acestora avand ca efect scaderea selectivitatii de forma. Insa, studii recente au pus in evidenta faptul ca reactiile care au loc pe suprafata externa a catalizatorilor zeolitici si /sau la gura porilor sunt foarte selective, sugerandu-se existenta unei "selectivitati de forma" in functie de natura substratului.
In separarea moleculelor dupa dimensiuni in cazul catalizei pe zeoliti un rol hotarator il are natura acestora, respectiv arhitectura porilor. Intr-o forma simplista cataliza selectiva de forma se poate defini ca imposibilitatea unor molecule din amestecul de reactanti de a accede in interiorul porilor (selectivitate de reactant) sau a unor molecule de produsi de reactie de a parasi porii (selectivitatea de produs). In practica insa, selectivitatea de reactanti sau produsi nu se manifesta doar in cazul in care moleculele au dimensiuni mai mari decat diametrul porilor (excludere dupa dimensiuni) ci si atunci cand vitezele de difuzie ale acestora sunt mai mici decat ale altor molecule (pentru valori concludente diferentele de selectivitate dintre molecule participante la reactie trebuie sa fie de cel putin doua ordine de marime). Diferentele dintre vitezele relative de reactie si difuzie sunt datorate interactiunilor de natura fizica si chimica dintre speciile participante la transformarea chimica.
In cazul in care dimensiunile moleculelor participante la reactie sunt apropiate de diametrul porilor zeolitici se realizeaza un nou tip de difuzie (diferita de difuzia Knudsen sau difuzia moleculara), denumita difuzie configurationala care poate aduce modificari importante ale difuzivitatii. Astfel, pe zeolitul CaA, difuzivitatea trans - 2 - butenei este de 200 de ori mai mare comparativ cu cea a cis - 2 - butenei, desi diferenta dintre dimensiunile celor doi izomeri este de doar 0,2 Ǻ.
Natura suprafetelor intracristaline ale zeolitilor difera foarte mult de la puternic hidrofila (in cazul zeolitilor cu raport Si /Al mic) la slab hidrofila (hidrofoba) (pentru zeolitii cu raport Si /Al mare), fapt care influenteaza in mod semnificativ adsorbtia moleculelor polare si nepolare.
Selectivitatea de reactant a stat la baza punerii in practica a procesului Selectoforming. n-Alcanii din benzina usoara (n-C5 si n-C6) pot patrunde in interiorul porilor erionitului fiind transformate in propan si butan, iar moleculele izo-alcanilor corespunzatori nu vor suferi nici o transformare.
Selectivitatea de produs joaca un rol hotarator intr-o serie de procese tehnologice de obtinere a p - dialchilbenzenilor cum ar fi: disproportionarea selectiva a toluenului (SDTP), alchilarea toluenului cu etena /etanol. In toate aceste procese pe langa p-xilen, care este produsul majoritar, se formeaza si o- si m-xilenul, dar datorita dimensiunilor acestia nu pot difuza prin porii catalizatorilor zeolitici (ZSM-5) spre suprafata externa a cristalitelor zeolitice.
Pe zeolitul ZSM-5 modificat, in cazul reactiei de disproportionare a toluenului, care are loc la temperaturi ridicate, coeficientul de difuzie al p-xilenului este de cateva ori mai mare comparativ cu cei ai o - si m - xilenului. Cu alte cuvinte in cazul sintezei di-alchilbenzenilor izomerii orto si meta mai voluminosi vor suferi rapid reactii de izomerizare, transformandu-se in izomeri para eliminandu-se in felul acesta din porii catalizatorului.
In alte cazuri moleculele voluminoase se transforma cu viteze foarte mici in molecule cu diametre cinetice care sa nu le permita difuzia prin porii catalizatorilor zeolitici, iar prin acumularea acestora se formeaza cocsul, care produce dezactivarea acestora. In cazul cocsarii zeolitilor de tip MOR a fost propus asa - numitul mecanism al selectivitatii inverse: moleculele ramificate formate in supercavitati (care au diametrul de 1,3 nm) nu pot difuza prin porii de acces care au diametrul de 0,7 nm, in felul acesta se formeaza cocsul care limiteaza /blocheaza accesul moleculelor reactante spre centrele active.
Selectivitatea datorata efectului de sita moleculara, depinde de: vitezele relative de difuzie si de reactie, de dimensiunile moleculelor implicate in reactiile respective precum si de caracteristicile centrelor active (concentratia, numarul si taria acestora). In mod evident viteza de difuzie depinde de dimensiunea cristalitelor zeolitice, respectiv de dimensiunea "drumului de difuzie". Imbunatatirea selectivitatii catalizatorilor zeolitici se poate realiza prin alegerea unor conditii de lucru adecvate (temperatura are un rol hotarator asupra vitezei de reactie) si /sau prin ajustarea caracteristicilor acestora. De exemplu, in cazul disproportionarii toluenului, selectivitatea catalizatorului HZSM-5 fata de p - xilen este marita prin depunerea pe suprafata exterioara a cristalitelor zeolitice de Si, Mg, cocs, etc., care limiteaza desorbtia izomerilor meta si orto; acest efect este datorat partial si dezactivarii selective a centrelor acide situate pe suprafata externa a cristalitelor.
Selectivitatea de stare de tranzitie (spatioselectivitatea) apare atunci cand formarea intermediarilor de reactie sau a starilor de tranzitie, este limitata de spatiul disponibil din jurul centrelor active in general si de spatiul din porii zeolitici in particular. Cu alte cuvinte, spatioselectivitatea depinde de dimensiunile si forma: porilor, de dimensiunile intersectiilor acestora si a cavitatilor zeolitice. Selectivitatea de stare de tranzitie a fost propusa pentru prima data de catre Csicsery pentru a explica absenta 1,3,5 - trialchilbenzenilor in produsii de disproportionare a dialchilbenzenilor pe H-MOR, desi dimensiunile acestora le permit sa difuzeze prin porii zeolitici. Spatiul disponibil din canalele zeolitului H-MOR nu este suficient de mare pentru a gazdui intermediarii de tip difenilmetan, implicati in formarea 1,3,5 - trialchilbenzenilor, care sunt mai voluminosi decat cei implicati in formarea 1,2,3 - si 1,2,4 - trialchilbenzenilor.
Spre deosebire de selectivitatea datorata efectului de sita moleculara, spatioselectivitatea nu depinde de viteza de reactie si /sau difuzie. Acest lucru este evidentiat de faptul ca modificarea dimensiunilor cristalitelor zeolitice nu afecteaza spatioselectivitatea, dar influenteaza in mod hotarator selectivitatea datorata proprietatilor de sita moleculara. Cele doua tipuri de selectivitate pot actiona simultan ca in cazul izopropilarii naftalinei pe H-MOR.
Avand in vedere ca marea majoritate a compusilor sufera simultan transformari monomoleculare (intramoleculare) si /sau bimoleculare (intermoleculare), atunci este usor de inteles faptul ca forma si dimensiunile spatiului in care se afla situate centrele active influenteaza in mod hotarator selectivitatea acestor transformari. Starile de tranzitie (intermediare) corespunzatoare reactiilor bimoleculare sunt mai voluminoase decat cele corespunzatoare reactiilor monomoleculare si in consecinta primele reactii sunt mai sensibile la constrangerilor sterice exercitate de catre peretii porilor zeolitici asupra intermediarilor de reactie. Acest fapt explica rolul cheie jucat de structura porilor zeolitici asupra selectivitatii in foarte multe transformari chimice. Un exemplu in acest sens il constituie izomerizarea selectiva a xilenilor pe zeolitii HZSM-5, cand intermediarii de reactie voluminosi rezultati din reactiile secundare nu se pot forma la intersectiile porilor. In cazul in care o reactie poate avea loc atat printr-un mecanism monomolecular cat si bimolecular, importanta celui de al doilea scade cu dimensiunea spatiului din jurul centrelor active. Spatioselectivitatea joaca un rol important in formarea produsilor cu masa moleculara mare, implicati in formarea cocsului, deoarece mecanismul de formare al acestuia presupune mai multe etape bimoleculare (condensare, transfer de hidrogen, etc.) foarte sensibile la constrangerile sterice exercitate de peretii porilor si /sau cavitatilor. Cu alte cuvinte formarea cocsului este influentata pe de o parte de dimensiunea si forma porilor si /sau cavitatilor iar pe alta parte de selectivitatea de forma inversa.
Selectivitatea de forma si concentratia moleculelor din porii catalizatorilor zeolitici. Interactiunile dintre moleculele organice si peretii porilor sunt foarte puternice (fiind caracterizate de izoterme de tip I, Langmuir) astfel incat, zeolitii pot fi considerati ca fiind solventi solizi. Concentratia reactantilor in microporii zeolitici este considerabil mai mare decat in faza gazoasa, fapt care are o influenta pozitiva asupra vitezei de reactie, efect care este mai pronuntat odata cu cresterea ordinului de reactie, fiind favorizate reactiile bimoleculare comparativ cu cele monomoleculare.
Concentratia moleculelor reactante din porii zeolitici este responsabila in mare parte si de faptul ca zeolitii sunt mai activi comparativ cu ceilalti catalizatori conventionali. Un astfel de exemplu il constituie catalizatorul de cracare catalitica REHY utilizat in procesul FCC (cracare catalitica in strat fluidizat), care in functie de natura hidrocarburilor din materia prima este de 10 -10.000 ori mai activ decat catalizatorii amorfi de alumino - silice; selectivitatile obtinute sunt de asemenea total diferite, benzina obtinuta pe catalizatorii zeolitici fiind bogata in hidrocarburi aromatice si alcani fata de cea obtinuta pe Al2O3 . SiO2 care este bogata in naftene si alchene. Aceasta modificare drastica a selectivitatii este datorata raportului diferit dintre vitezele reactiilor de transfer de hidrogen (bimoleculare) si cea reactiilor de cracare, care este mult mai mare pe zeoliti decat pe alumosilice. Randamentele mai mari in benzina obtinute pe catalizatorii zeolitici se datoreaza in primul rand faptului ca hidrocarburile aromatice si alcanii sunt mai refractare fata de reactiile de cracare secundare.
In unele cazuri concentratiile mari ale unuia dintre reactanti in porii catalizatorilor zeolitici pot determina aparitia unor reactii nedorite. Un astfel de exemplu este cel al alchilarii i-butanului cu butene, reactie in care zeolitii s-au dovedit foarte eficienti, insa datorita faptului ca alchenele sunt mai puternic adsorbite in porii zeolitici comparativ cu alcanii, paralel cu reactiile de alchilare au loc si reactiile de cocsare si oligomerizare. Pe langa tipurile de selectivitate mai sus mentionate au fost propuse si alte tipuri.
Efectul de cavitate sau efectul ferestrei a fost propus de catre Gorring pentru a explica efectul de "neliniaritate" al catenei in cazul hidrocracarii n-alcanilor pe zeolitii T, chabazit si erionit. Astfel, in cazul cracarii n-C22 pe erionit se observa doua maxime in distributia moleculelor produsilor de reactie in functie de numarul atomilor de C la 4 si respectiv 11 si un minim la C 8, iar valorile difuzivitatilor se modifica in mod corespunzator (cu cel putin doua ordine de marime) de la minim la C 8 la maxim la C 4 si C11. Cu alte cuvinte pentru a se obtine selectivitati cat mai mari trebuie avute in vedere si dimensiunile si structurile moleculelor reactante si produsilor de reactie.
Conceptul de control al traficului molecular a fost propus de
catre Derouane si Gabelica pentru a explica absenta efectelor
contradifuziei in cazul conversiei metanolului pe zeoliti
Fraenkel si
colab. au fost primii care au sugerat implicarea suprafetei
externe a catalizatorilor zeolitici in cataliza selectiva de forma.
Astfel, centrele acide localizate pe semicavitatile de pe
suprafata externa a zeolitilor HMFI, sunt responsabile pentru
formarea 2,6 - si 2,7 - dimetilnaftalinei in cazul reactiei de
metilare a naftalinei (efect "cuibar" - nest efect). Aceasta idee a fost
respinsa pe baza rezultatelor de adsorbtie, insa efectul de
cuibar a fost propus recent din nou pentru a se explica selectivitatea de
forma a sitei moleculare
Posibilitatea desfasurarii reactiilor chimice pe suprafata externa a catalizatorilor zeolitici, mai exact la "gura porilor" a fost avansata pentru prima data de catre Martens si colab. pentru a explica selectivitatea neobisnuita manifestata de unii zeoliti cu pori medii (ZSM-22 - TON) in reactia de izomerizare a n-alcanilor cu catene lungi. PePt-HZSM-22 reactia decurge cu selectivitate mare fata de izomerii monoramificati desi, acestia nu se pot desorbi din canalele monodimensionale inguste ale zeolitului.
Cataliza la "gura porilor" poate fi de asemenea responsabila de izomerizarea selectiva a n-butenei la i-butena pe HFER. In acest caz, compusii hidrocarbonati captati in porii din vecinatatea suprafetei externe au fost considerati ca fiind speciile active.
Ulterior, s-a constatat ca reactiile secundare de ramificare a n-alcanilor pePt-HTON au loc in pozitii determinate de deschiderile porilor de pe suprafata externa a cristalitelor zeolitice. Acest tip de selectivitate a fost denumita selectivitate de tip "cheie - broasca /yala) fiind asemanatoare cu cataliza enzimatica. Acest concept a fost utilizat de catre Derouane si Vanderveken pentru a explica aromatizarea selectiva a n-C6 pe Pt-LTL, "efectele de captivitate" a intermediarilor de reactie in interiorul porilor cu structura specifica zeolitului LTL fiind considerate responsabile pentru conversia selectiva a n-hexanului in benzen.
Zeolitii, sunt total deosebiti de alte tipuri de catalizatori prin aceea ca centrele lor acide, se gasesc situate pe suprafata intracristalina (in cavitati si canale) si sunt asociati cu atomii de Al coordinati tetraedric din reteaua cristalina.
Aciditatea
zeolitilor cu pori medii si raport SiO2 /Al2O3
mare, pare la prima vedere o problema mult mai usor de elucidat, mai
putin complicata. Astfel, chiar din 1980, Olson, a gasit, pentru probe de zeolit
HZSM-5 cu raport molar SiO2/Al2O3 cuprins
intre 35-60.000 (![]() 15 ppm Al), ca intre activitatea catalitica si numarul
de centre acide (protonice) se stabileste o variatie liniara
(fig.III.4.). La acest rezultat s-a
ajuns folosind asa numitul test
15 ppm Al), ca intre activitatea catalitica si numarul
de centre acide (protonice) se stabileste o variatie liniara
(fig.III.4.). La acest rezultat s-a
ajuns folosind asa numitul test ![]() .
.
α
![]()
![]()
![]()
![]()


![]()
![]() 100 x[Al/(Al+Si)]
100 x[Al/(Al+Si)]
![]()
![]()
![]() 200 2,0
200 2,0
![]()
![]()
![]()
![]() 150
150
![]()
![]()
![]() 1,0
1,0
![]()
![]() 50
50
![]()
![]()
![]()
![]()
![]()
Semnal RMN-27Al 100 x[Al/(Al+Si)], RMN
![]()
![]() Fig. III.4
Relatia intre activitatea catalitica, analiza elementara si
semnalul Al
Fig. III.4
Relatia intre activitatea catalitica, analiza elementara si
semnalul Al ![]() ) functie de semnalul relativ Al
) functie de semnalul relativ Al
Relatii
asemanatoare au fost gasite pentru alte reactii acid
catalizate de acesti zeoliti, si anume: disproportionarea
toluenului, conversia metanolului la hidrocarburi, dezalchilarea
etilbenzenului, izomerizarea ciclopropanului, izomerizarea, xilenului, cracarea
cumenului.Rezultatele obtinute prin analiza elementara, spectroscopie
IR, TPD, Al